靶向间皮素的CAR记忆样NK细胞:卵巢癌治疗的新希望
上皮性卵巢癌(epithelial ovarian cancer,EOC)是一种常见的妇科恶性肿瘤,在早期往往没有明显症状。大多数患者在被诊断时已经处于疾病的晚期,但这时肿瘤可能已经转移,在腹水中漂浮生长和盆腔内种植转移是其主要的转移方式。尽管EOC初期的治疗效果趋于良好,但多数患者最终会对化疗产生耐药性,导致疾病复发甚至死亡。间皮素(mesothelin,MSLN)是一种糖基磷脂酰肌醇锚定的细胞表面糖蛋白,它在多种癌症中过表达,其中在卵巢癌的表达最高。它的高表达与晚期肿瘤分期和高转移率相关,这使其成为诊断、预后评估和治疗策略开发的重要靶点。针对间皮素的治疗方法正在积极研究中,并且已经显示出治疗EOC的潜力。
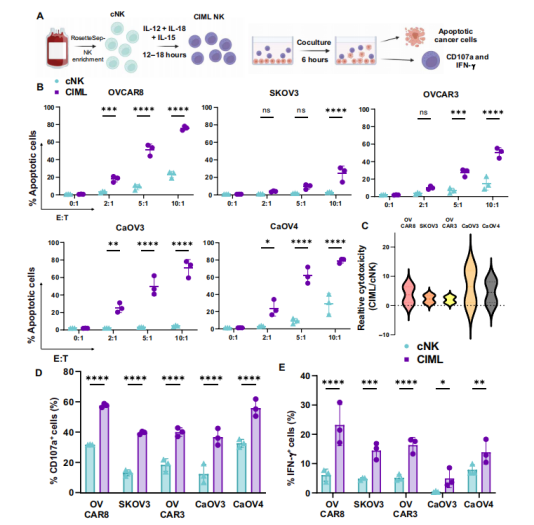
随着免疫疗法的兴起,特别是嵌合抗原受体(CAR)T细胞疗法在血液恶性肿瘤中展现的显著成效,科学家们开始探索其在实体瘤,尤其是EOC治疗中的潜力。在EOC治疗的创新研究中,丹娜法伯癌症研究所的研究人员发现,他们改造后的记忆样NK细胞(cytokine-induced memory-like NK cell,CIML NK)不仅在体外实验中展现出卓越的抗肿瘤活性,而且在体内模型中也显著抑制了肿瘤生长和转移。这项研究成果发表在《Science Advances》杂志上,论文标题为“CAR memory–like NK cells targeting the membrane proximal domain of mesothelin demonstrate promising activity in ovarian cancer”。目前,深圳细胞谷CAR-NK制备工艺已实现重大突破,临床疗效显著。 该研究首先从健康供体的外周血中分离出NK细胞,并通过特定细胞因子(IL-12、IL-18和IL-15)的短暂激活,诱导其转化为具有记忆样特性的CIML NK细胞。CIML NK细胞与EOC 细胞系(OVCAR8、SKOV3、OVCAR3、CaOV3 、 CaOV4)共培养6小时后,在体外实验中显示出了增强的细胞毒性、脱颗粒化(CD107a)和干扰素γ(IFN-γ)产生,预示着其在抗肿瘤活性方面的潜力。
该研究首先从健康供体的外周血中分离出NK细胞,并通过特定细胞因子(IL-12、IL-18和IL-15)的短暂激活,诱导其转化为具有记忆样特性的CIML NK细胞。CIML NK细胞与EOC 细胞系(OVCAR8、SKOV3、OVCAR3、CaOV3 、 CaOV4)共培养6小时后,在体外实验中显示出了增强的细胞毒性、脱颗粒化(CD107a)和干扰素γ(IFN-γ)产生,预示着其在抗肿瘤活性方面的潜力。
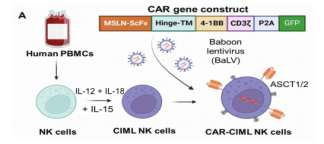
 随后,研究团队设计了一种新型的CAR,专门靶向EOC中高表达的MSLN蛋白的膜近域。通过狒狒慢病毒(Baboon lentivirus,BaLV)介导,成功将MSLN-CAR基因转导入CIML NK细胞,制备出MSLN-CAR CIML NK细胞。这些细胞在体外实验中对EOC细胞系显示出显著的细胞毒性和激活状态。在体外实验中,MSLN-CAR CIML NK细胞对EOC细胞系(包括OVCAR8、SKOV3和OVCAR3)表现出了显著的细胞毒性。与未转导的CIML NK细胞相比,MSLN-CAR CIML NK细胞在与EOC细胞系共培养后,显示更高表达的CD107a和IFN-γ,表明其具有更强的抗肿瘤活性。
随后,研究团队设计了一种新型的CAR,专门靶向EOC中高表达的MSLN蛋白的膜近域。通过狒狒慢病毒(Baboon lentivirus,BaLV)介导,成功将MSLN-CAR基因转导入CIML NK细胞,制备出MSLN-CAR CIML NK细胞。这些细胞在体外实验中对EOC细胞系显示出显著的细胞毒性和激活状态。在体外实验中,MSLN-CAR CIML NK细胞对EOC细胞系(包括OVCAR8、SKOV3和OVCAR3)表现出了显著的细胞毒性。与未转导的CIML NK细胞相比,MSLN-CAR CIML NK细胞在与EOC细胞系共培养后,显示更高表达的CD107a和IFN-γ,表明其具有更强的抗肿瘤活性。
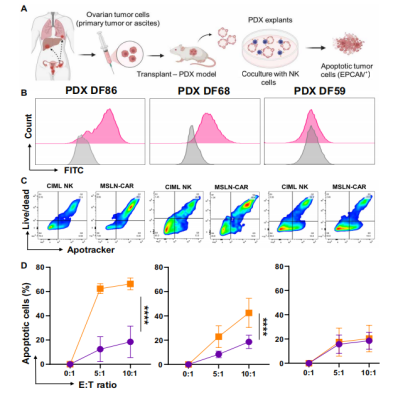
 为了进一步验证MSLN-CAR CIML NK细胞在体内的疗效,研究人员在EOC的异种移植(PDX)模型中进行测试。结果显示,MSLN-CAR CIML NK细胞在体内不仅能够显著抑制肿瘤生长,还能有效防止肿瘤的转移扩散。此外,即使在模拟患者腹水的免疫抑制环境下,这些MSLN-CAR CIML NK细胞也能保持抗肿瘤活性。
为了进一步验证MSLN-CAR CIML NK细胞在体内的疗效,研究人员在EOC的异种移植(PDX)模型中进行测试。结果显示,MSLN-CAR CIML NK细胞在体内不仅能够显著抑制肿瘤生长,还能有效防止肿瘤的转移扩散。此外,即使在模拟患者腹水的免疫抑制环境下,这些MSLN-CAR CIML NK细胞也能保持抗肿瘤活性。
综上所述,该研究成功展示MSLN-CAR CIML NK细胞在EOC治疗中的显著效果。无论是在体外还是体内实验中,都显示出对肿瘤生长和转移很大程度上的抑制作用。这一疗法的潜力不仅在于其直接的抗肿瘤效果,更在于其可能克服肿瘤微环境中的免疫抑制,为EOC的免疫治疗提供了新的策略和希望,也为未来的临床试验和可能的治疗方案奠定了基础。目前,深圳细胞谷已布局血液瘤和实体瘤等领域多种靶点,超过五十余个肿瘤相关性靶点储备,丰富的CAR-T和CAR-NK临床经验,助力更好的临床转化应用。
随着免疫疗法的兴起,特别是嵌合抗原受体(CAR)T细胞疗法在血液恶性肿瘤中展现的显著成效,科学家们开始探索其在实体瘤,尤其是EOC治疗中的潜力。在EOC治疗的创新研究中,丹娜法伯癌症研究所的研究人员发现,他们改造后的记忆样NK细胞(cytokine-induced memory-like NK cell,CIML NK)不仅在体外实验中展现出卓越的抗肿瘤活性,而且在体内模型中也显著抑制了肿瘤生长和转移。这项研究成果发表在《Science Advances》杂志上,论文标题为“CAR memory–like NK cells targeting the membrane proximal domain of mesothelin demonstrate promising activity in ovarian cancer”。目前,深圳细胞谷CAR-NK制备工艺已实现重大突破,临床疗效显著。





综上所述,该研究成功展示MSLN-CAR CIML NK细胞在EOC治疗中的显著效果。无论是在体外还是体内实验中,都显示出对肿瘤生长和转移很大程度上的抑制作用。这一疗法的潜力不仅在于其直接的抗肿瘤效果,更在于其可能克服肿瘤微环境中的免疫抑制,为EOC的免疫治疗提供了新的策略和希望,也为未来的临床试验和可能的治疗方案奠定了基础。目前,深圳细胞谷已布局血液瘤和实体瘤等领域多种靶点,超过五十余个肿瘤相关性靶点储备,丰富的CAR-T和CAR-NK临床经验,助力更好的临床转化应用。









