细胞免疫疗法在自身免疫性疾病中的应用
自身免疫性疾病(autoimmune diseases,ADs)是由于自身抗原免疫耐受紊乱、机体对自身抗原发生免疫反应导致机体损害的一类疾病(图1)。因此,ADs本质上是一种免疫失衡和混乱,是由于人体免疫系统错误地攻击自身成分而发生的一系列疾病。ADs包括器官特异性ADs和系统性ADs。器官特异性ADs是指患者的病变一般局限于某一特定的器官,由针对特定器官的自身免疫反应引起,主要包括桥本甲状腺炎、Graves病、重症肌无力等。系统性ADs是指免疫反应造成全身多器官和组织的病理损伤,主要包括类风湿性关节炎(RA)、系统性红斑狼疮(SLE)、干燥综合征(SS)等[1]。
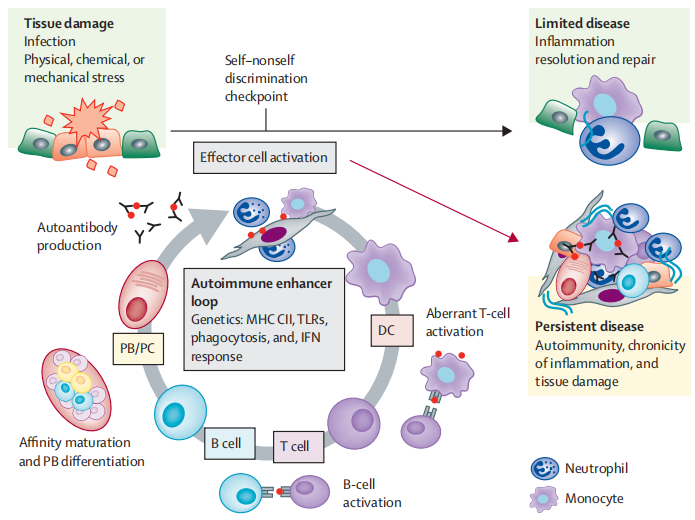
图1: 自身免疫环路触发慢性炎症和组织损伤
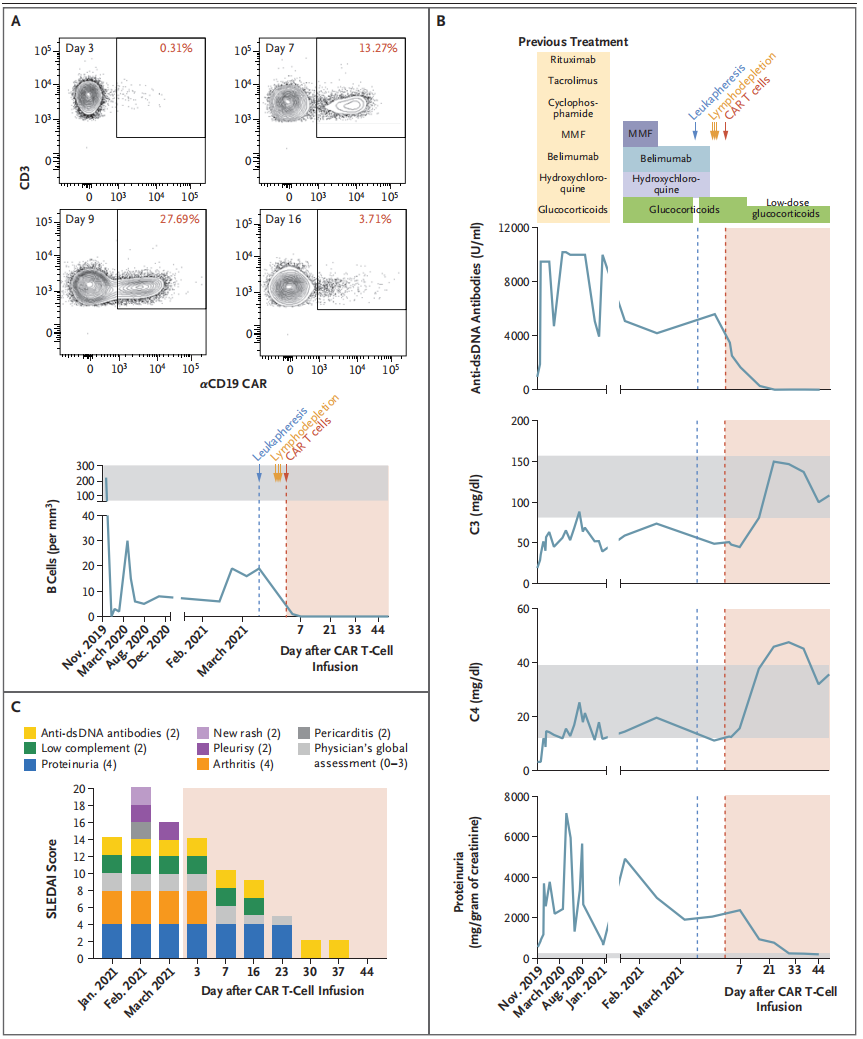
图2:CAR-T细胞疗法应用于系统性红斑狼疮的治疗结果
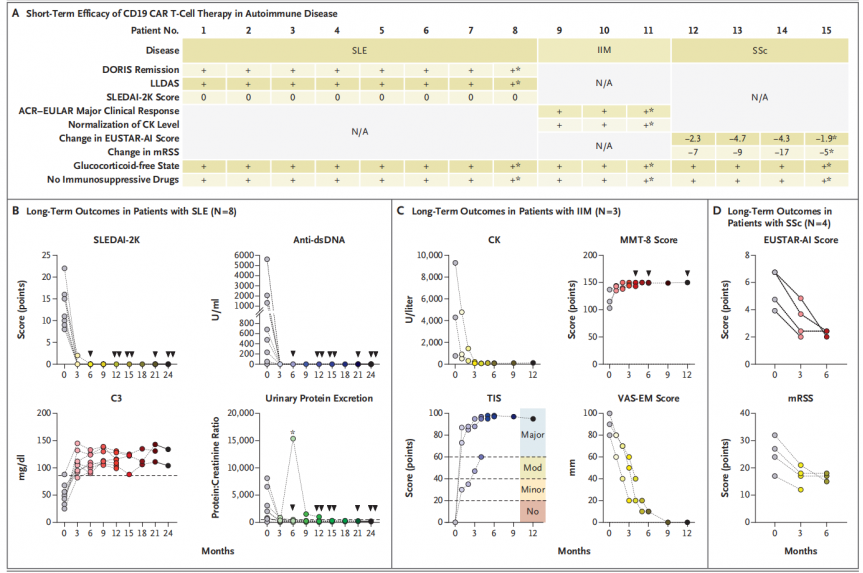
图3:CD19 CAR T细胞疗法在自身免疫性疾病中的临床疗效
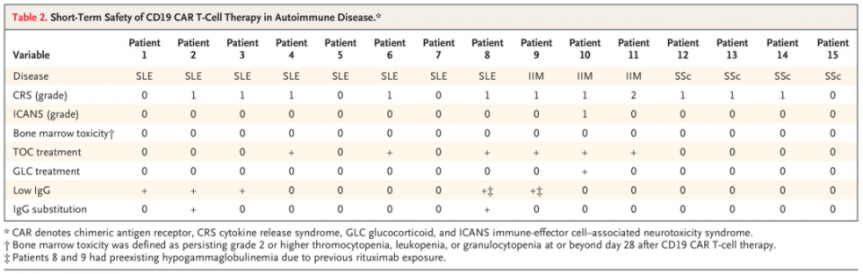
图4:CD19 CAR-T细胞疗法在自身免疫性疾病中的短期安全性
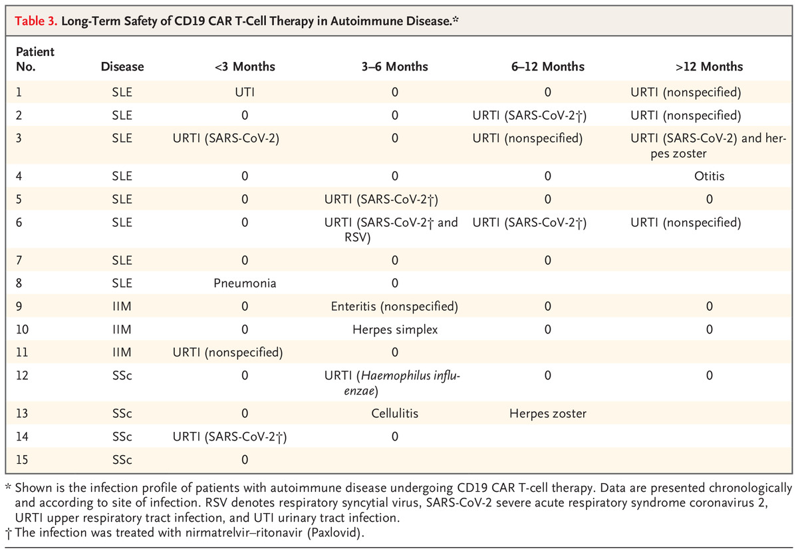
图5:CD19 CAR-T细胞疗法在自身免疫性疾病中的长期安全性
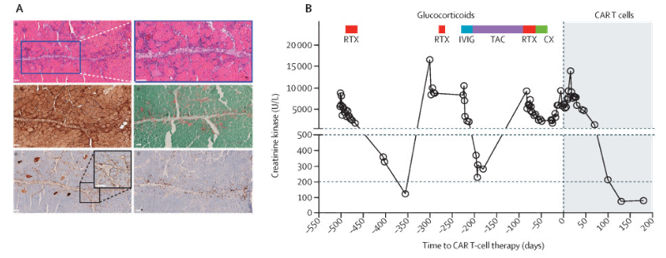
图6:抗合成酶综合征的体征
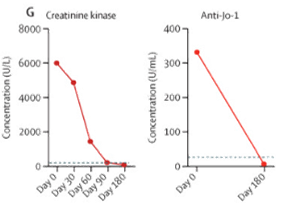
图7:CAR T细胞处理后肌酐激酶浓度变化
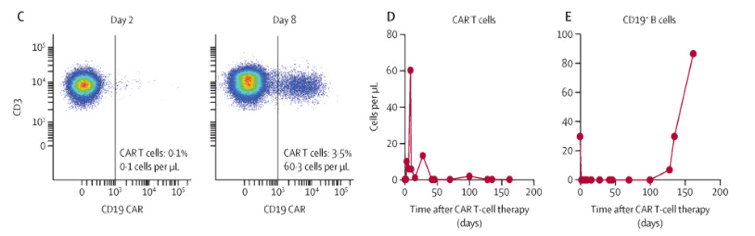
图8:CAR T细胞的数量在体内的变化
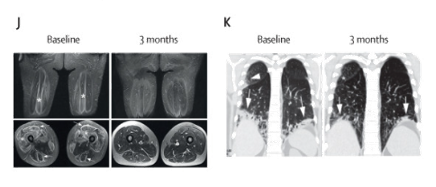
图9:患者肌炎的病变完全消退且呼吸道症状有所改善
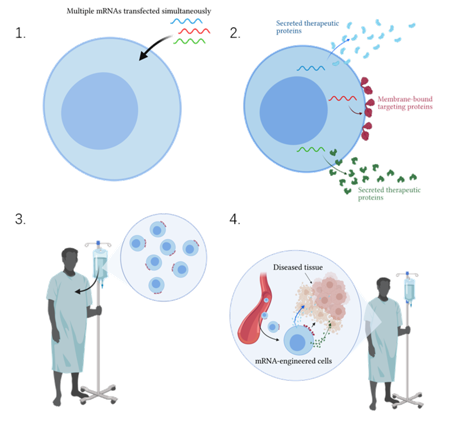
图10:Cartesian的RNA Armory技术平台工作原理
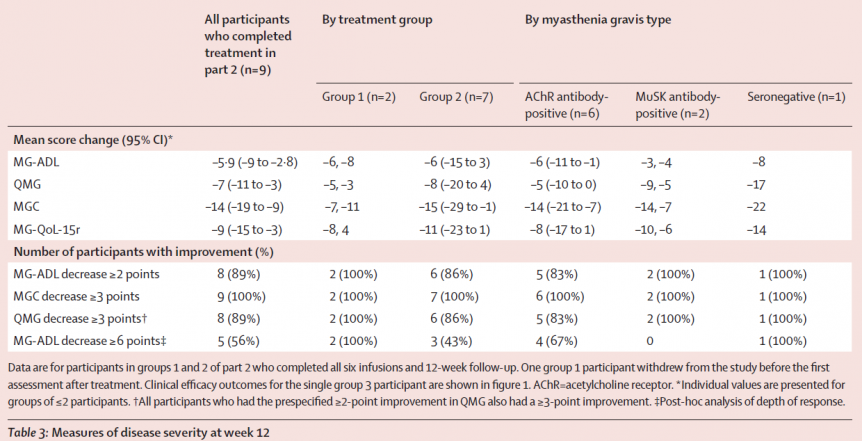
图11:接受治疗12周时疾病严重程度指标的改变

图1: 自身免疫环路触发慢性炎症和组织损伤
目前,自身免疫性疾病主要由广泛的免疫抑制剂和阻断抗体治疗,这些药物可以控制疾病,但通常不能治愈。靶向CD19的嵌合抗原受体CAR-T细胞在B细胞恶性肿瘤中非常有效。同时,CD19 CAR-T细胞也靶向触发自身免疫性疾病(AID)的自身反应性B细胞,包括系统性红斑狼疮(SLE)、特发性炎症性肌炎(IIM)和系统性硬化症(SSc)。
1、靶向CD19的CAR-T治疗系统性红斑狼疮
对于系统性红斑狼疮,患者包括双链DNA(dsDNA)和核蛋白在内的核抗原的免疫耐受性被破坏,导致T淋巴细胞减少、抑制性T细胞功能降低、B细胞过度增生,从而产生大量针对dsDNA和其他核抗原的自身抗体。由于B细胞对DNA和核抗原的反应要先于临床症状的出现,因此,通过B细胞耗竭来治疗系统性红斑狼疮是一种有吸引力的新策略。
早在2021年8月5日,德国埃尔朗根-纽伦堡大学(FAU)的 Georg Schett 教授等人在《新英格兰医学杂志》(NEJM)上发表临床研究论文:CD19-Targeted CAR T Cells in Refractory Systemic Lupus Erythematosus[2],首次将CAR-T细胞疗法应用于系统性红斑狼疮的治疗,并成功治疗了一名年轻女性患者。结果显示(图2),从自身免疫疾病的患者中生产CAR-T细胞是可行的,同时,患者对CAR-T细胞输注具有良好的耐受性,且没有导致任何严重的毒性作用。这种治疗方法使体内B细胞快速清除,同时伴随着外周血中CAR-T细胞的快速扩增。患者3个月后症状缓解,所有免疫抑制剂(包括糖皮质激素)均已停用,并在18个月内无疾病复发迹象。
1、靶向CD19的CAR-T治疗系统性红斑狼疮
对于系统性红斑狼疮,患者包括双链DNA(dsDNA)和核蛋白在内的核抗原的免疫耐受性被破坏,导致T淋巴细胞减少、抑制性T细胞功能降低、B细胞过度增生,从而产生大量针对dsDNA和其他核抗原的自身抗体。由于B细胞对DNA和核抗原的反应要先于临床症状的出现,因此,通过B细胞耗竭来治疗系统性红斑狼疮是一种有吸引力的新策略。
早在2021年8月5日,德国埃尔朗根-纽伦堡大学(FAU)的 Georg Schett 教授等人在《新英格兰医学杂志》(NEJM)上发表临床研究论文:CD19-Targeted CAR T Cells in Refractory Systemic Lupus Erythematosus[2],首次将CAR-T细胞疗法应用于系统性红斑狼疮的治疗,并成功治疗了一名年轻女性患者。结果显示(图2),从自身免疫疾病的患者中生产CAR-T细胞是可行的,同时,患者对CAR-T细胞输注具有良好的耐受性,且没有导致任何严重的毒性作用。这种治疗方法使体内B细胞快速清除,同时伴随着外周血中CAR-T细胞的快速扩增。患者3个月后症状缓解,所有免疫抑制剂(包括糖皮质激素)均已停用,并在18个月内无疾病复发迹象。

图2:CAR-T细胞疗法应用于系统性红斑狼疮的治疗结果
在2024年2月22日医学界顶级期刊《新英格兰医学杂志》发表了一篇15例样本量CD19 CAR-T细胞治疗自身免疫性疾病的论著,题目为CD19 CAR T-Cell Therapy in Autoimmune Disease — A Case Series with Follow-up[3]。文中评估了15名患有严重系统性红斑狼疮(8名患者)、特发性炎性肌病(3名患者)或系统性硬化症(4名患者)的患者,在用氟达拉滨和环磷酰胺进行预处理后,接受了单次CD19 CAR-T细胞输注。这些患者在输注CAR-T后接受中位随访15个月(范围为 4 至 29 个月)后,所有8名SLE患者均根据SLE缓解定义(DORIS)缓解标准实现了疾病缓解。所有4名SSC患者的欧洲硬皮病试验和研究组活动指数的得分也有所下降,表明疾病活动度较低(图3)。

图3:CD19 CAR T细胞疗法在自身免疫性疾病中的临床疗效
在安全性方面,该疗法总体耐受性良好。10例患者出现轻度细胞因子释放综合征(CAR-T疗法的炎症副作用),1例患者出现中度细胞因子释放综合征,1例患者出现眩晕。没有报告与治疗相关的严重不良事件。

图4:CD19 CAR-T细胞疗法在自身免疫性疾病中的短期安全性

图5:CD19 CAR-T细胞疗法在自身免疫性疾病中的长期安全性
在该病例系列中,CD19 CAR-T细胞转移在三种不同的自身免疫性疾病中似乎是可行、安全和有效的,为进一步的对照临床试验提供了依据(图4、图5)。
2、靶向CD19的CAR-T治疗难治性抗合成酶综合征
2023年2月,Georg Schett 团队等人在《柳叶刀》发表临床研究论文:CD19-targeted CAR-T cells in refractory antisynthetase syndrome[4],使用CAR-T细胞疗法成功治疗了一种新的自身免疫疾病——特发性炎性肌病。
这名患者患有自身免疫疾病特发性炎性肌病的亚型——抗合成酶抗体综合征(图6)。这是一种严重的自身免疫性炎症性肌肉疾病,该疾病是由于体内参与氨基酸合成的氨酰-tRNA合成酶被免疫系统错误攻击所导致的,从而影响各种细胞的功能。
2、靶向CD19的CAR-T治疗难治性抗合成酶综合征
2023年2月,Georg Schett 团队等人在《柳叶刀》发表临床研究论文:CD19-targeted CAR-T cells in refractory antisynthetase syndrome[4],使用CAR-T细胞疗法成功治疗了一种新的自身免疫疾病——特发性炎性肌病。
这名患者患有自身免疫疾病特发性炎性肌病的亚型——抗合成酶抗体综合征(图6)。这是一种严重的自身免疫性炎症性肌肉疾病,该疾病是由于体内参与氨基酸合成的氨酰-tRNA合成酶被免疫系统错误攻击所导致的,从而影响各种细胞的功能。

图6:抗合成酶综合征的体征

图7:CAR T细胞处理后肌酐激酶浓度变化

图8:CAR T细胞的数量在体内的变化

图9:患者肌炎的病变完全消退且呼吸道症状有所改善
这是世界首个使用CAR-T细胞疗法成功治疗的抗合成酶抗体综合征患者,也是继系统性红斑狼疮后,第二种被CAR-T成功治疗的自身免疫疾病。
3、靶向BCMA的rCAR-T治疗重症肌无力
重症肌无力(Myasthenia Gravis,MG)是一种神经系统的自身免疫性疾病,最常见的原因是身体的免疫系统攻击了神经细胞与肌肉信息交流处的蛋白,导致肌肉无力。
CAR-T细胞疗法可能会产生严重副作用,这对于晚期癌症患者而言能够接受,但对重症肌无力这种慢性自身免疫性疾病而言似乎不值得冒险。通常情况下,通过向T细胞递送并整合DNA来构建CAR-T细胞,这导致递送的DNA在T细胞中持续存在,且会随着细胞分裂而复制,这可能导致放大效应和严重副作用。
为了避免CAR-T细胞疗法的这种副作用,Cartesian Therapeutics 开发了一种使用mRNA代替DNA对T细胞进行重编程改造的新平台——RNA Armory®,通过脂质纳米颗粒(LNP)递送的mRNA不会在T细胞基因组中整合,因此不会随细胞分裂而复制。这种基于mRNA的CAR-T细胞疗法是一种短期疗法,需要多次重复注射。
Cartesian公司开发的DESCARTES-08的疗法(图10),是首个基于RNA的CAR-T细胞(rCAR-T)治疗自身免疫性疾病的新疗法,并首次推进到了临床试验中,这项临床试验旨在确定理想剂量,有效减轻重症肌无力患者的肌肉无力症状,并将副作用降到最低。
3、靶向BCMA的rCAR-T治疗重症肌无力
重症肌无力(Myasthenia Gravis,MG)是一种神经系统的自身免疫性疾病,最常见的原因是身体的免疫系统攻击了神经细胞与肌肉信息交流处的蛋白,导致肌肉无力。
CAR-T细胞疗法可能会产生严重副作用,这对于晚期癌症患者而言能够接受,但对重症肌无力这种慢性自身免疫性疾病而言似乎不值得冒险。通常情况下,通过向T细胞递送并整合DNA来构建CAR-T细胞,这导致递送的DNA在T细胞中持续存在,且会随着细胞分裂而复制,这可能导致放大效应和严重副作用。
为了避免CAR-T细胞疗法的这种副作用,Cartesian Therapeutics 开发了一种使用mRNA代替DNA对T细胞进行重编程改造的新平台——RNA Armory®,通过脂质纳米颗粒(LNP)递送的mRNA不会在T细胞基因组中整合,因此不会随细胞分裂而复制。这种基于mRNA的CAR-T细胞疗法是一种短期疗法,需要多次重复注射。
Cartesian公司开发的DESCARTES-08的疗法(图10),是首个基于RNA的CAR-T细胞(rCAR-T)治疗自身免疫性疾病的新疗法,并首次推进到了临床试验中,这项临床试验旨在确定理想剂量,有效减轻重症肌无力患者的肌肉无力症状,并将副作用降到最低。

图10:Cartesian的RNA Armory技术平台工作原理
近日,加州大学欧文分校、北卡罗来纳大学教堂山分校、迈阿密大学和Cartesian公司的研究人员合作,在《The Lancet Neurology》期刊发表了题为:Safety and clinical activity of autologous RNA chimeric antigen receptor T-cell therapy in myasthenia gravis (MG-001): a prospective, multicentre, open-label, non-randomised phase 1b/2a study的研究论文[5]。
在这项临床试验中,共有14名患有广泛性重症肌无力的患者接受了不同剂量的rCAR-T细胞疗法(Descartes-08),靶向产生重症肌无力抗体的细胞。
3名患者在治疗后完全或近乎完全症状消除,并持续6个月无症状。2名患者不再需要慢性静脉注射免疫球蛋白治疗。治疗过程中没有出现剂量限制毒性、细胞因子释放综合征或神经毒性,常见的不良事件有头痛(6/14)、恶心(5/14)、呕吐(3/14)和发烧(4/14),这些不良事件在输注后24小时内消退。
在这项临床试验中,共有14名患有广泛性重症肌无力的患者接受了不同剂量的rCAR-T细胞疗法(Descartes-08),靶向产生重症肌无力抗体的细胞。
3名患者在治疗后完全或近乎完全症状消除,并持续6个月无症状。2名患者不再需要慢性静脉注射免疫球蛋白治疗。治疗过程中没有出现剂量限制毒性、细胞因子释放综合征或神经毒性,常见的不良事件有头痛(6/14)、恶心(5/14)、呕吐(3/14)和发烧(4/14),这些不良事件在输注后24小时内消退。

图11:接受治疗12周时疾病严重程度指标的改变
在这项首次针对自身免疫性疾病的rCAR-T细胞疗法临床试验中,Descartes-08总体上是安全且耐受性良好的。在输注后长达9个月的随访中,重症肌无力严重程度量表显示了有临床意义的下降(图11)。这提示了rCAR-T细胞疗法可作为一种潜在的治疗重症肌无力和其他自身免疫性疾病的新方法。
CAR-T细胞已经成功地应用于自身免疫性疾病的治疗中,这种方法的独特性,不仅因为它是有效的、个性化的转基因自体细胞产品,还因为其通过一次性干预获得长期无药物缓解,这种方法可能预示着自身免疫性疾病治疗的新时代,即将长期免疫抑制的当前治疗原则转化为一种不需要进一步治疗的免疫重置策略。针对CAR-T细胞治疗自身免疫性疾病的潜在应用仍需进一步研究,且已有大量研究正在进行中,并将更多地阐明这种治疗方法的潜力。
参考文献
1、J. D B ,Zoltan A ,A. J B , et al.CAR T therapy beyond cancer: the evolution of a living drug[J].Nature,2023,619(7971):707-715.
2、Dimitrios M ,Gerhard K ,Simon V , et al.CD19-Targeted CAR T Cells in Refractory Systemic Lupus Erythematosus[J].New England Journal of Medicine,2021,385(6):567-569.
3、Müller F ,Taubmann J ,Bucci L , et al.CD19 CAR T-Cell Therapy in Autoimmune Disease - A Case Series with Follow-up.[J].The New England journal of medicine,2024,390(8):687-700.
4、Fabian M ,Sebastian B ,Johannes K , et al.CD19-targeted CAR T cells in refractory antisynthetase syndrome[J].The Lancet,2023,401(10379):815-818.
5、Volkan G ,Michael B ,Metin K , et al.Safety and clinical activity of autologous RNA chimeric antigen receptor T-cell therapy in myasthenia gravis (MG-001): a prospective, multicentre, open-label, non-randomised phase 1b/2a study.[J].The Lancet. Neurology,2023,22(7):578-590.
免责声明:深圳细胞谷致力于研究细胞与基因疗法,为推动新兴技术,让更多人了解生物医药新发展。本文内容仅作信息交流使用,本平台对文中内容、陈述、观点判断保持中立,不代表深圳细胞谷立场和观点。本文相关信息不得用作诊断或治疗,不能代替专业医学意见,本公司网站将不承担任何责任。以上声明内容的最终解释权归本公司网站所有,本声明将适用本公司网站所有时间分享的文章,谢谢合作! 版权说明:文章版权归深圳细胞谷所有,欢迎个人转发发至朋友圈,媒体或机构在未经授权下,以任何形式转载载到其他平台,将视为侵权。如需转载,请联系邮箱:contact@sz-cell.com
CAR-T细胞已经成功地应用于自身免疫性疾病的治疗中,这种方法的独特性,不仅因为它是有效的、个性化的转基因自体细胞产品,还因为其通过一次性干预获得长期无药物缓解,这种方法可能预示着自身免疫性疾病治疗的新时代,即将长期免疫抑制的当前治疗原则转化为一种不需要进一步治疗的免疫重置策略。针对CAR-T细胞治疗自身免疫性疾病的潜在应用仍需进一步研究,且已有大量研究正在进行中,并将更多地阐明这种治疗方法的潜力。
参考文献
1、J. D B ,Zoltan A ,A. J B , et al.CAR T therapy beyond cancer: the evolution of a living drug[J].Nature,2023,619(7971):707-715.
2、Dimitrios M ,Gerhard K ,Simon V , et al.CD19-Targeted CAR T Cells in Refractory Systemic Lupus Erythematosus[J].New England Journal of Medicine,2021,385(6):567-569.
3、Müller F ,Taubmann J ,Bucci L , et al.CD19 CAR T-Cell Therapy in Autoimmune Disease - A Case Series with Follow-up.[J].The New England journal of medicine,2024,390(8):687-700.
4、Fabian M ,Sebastian B ,Johannes K , et al.CD19-targeted CAR T cells in refractory antisynthetase syndrome[J].The Lancet,2023,401(10379):815-818.
5、Volkan G ,Michael B ,Metin K , et al.Safety and clinical activity of autologous RNA chimeric antigen receptor T-cell therapy in myasthenia gravis (MG-001): a prospective, multicentre, open-label, non-randomised phase 1b/2a study.[J].The Lancet. Neurology,2023,22(7):578-590.
免责声明:深圳细胞谷致力于研究细胞与基因疗法,为推动新兴技术,让更多人了解生物医药新发展。本文内容仅作信息交流使用,本平台对文中内容、陈述、观点判断保持中立,不代表深圳细胞谷立场和观点。本文相关信息不得用作诊断或治疗,不能代替专业医学意见,本公司网站将不承担任何责任。以上声明内容的最终解释权归本公司网站所有,本声明将适用本公司网站所有时间分享的文章,谢谢合作! 版权说明:文章版权归深圳细胞谷所有,欢迎个人转发发至朋友圈,媒体或机构在未经授权下,以任何形式转载载到其他平台,将视为侵权。如需转载,请联系邮箱:contact@sz-cell.com









